近日,中南大学生命科学学院与湘雅医院合作在《癌症研究》(Cancer Research)在线发表题为“节律分子RORA通过抑制PD-L1表达增强黑素瘤免疫监视(The Circadian Clock Component RORA Increases Immunosurveillance in Melanoma by Inhibiting PD-L1 Expression)”的研究论文。该研究发现关键节律分子RORA与抗肿瘤免疫相关,RORA激活通过抑制PD-L1转录增强了细胞毒性T细胞活性,揭示了DEAD-box解旋酶家族成员DDX3X可以与HDAC3竞争结合RORA并上调PD-L1表达,从而发挥免疫抑制效应的分子机制。同时,该研究提出了RORA激动剂川陈皮素联合CTLA4抗体协同抑制黑素瘤生长的新策略。

生物钟紊乱与肥胖、自身免疫疾病和癌症等多种慢性疾病密切相关。来自癌症基因组图谱(TCGA)的人类数据显示,在多种不同癌症类型中,核心节律基因下调与致癌驱动途径、肿瘤分期和生存率存在显著相关性。节律基因CRY1、PER1、PER2和RORs的异常表达可促进肿瘤进展通过癌症相关过程,包括细胞增殖和DNA损伤反应。节律基因视黄酸受体相关孤儿受体-α(RORA)是一种潜在的肿瘤抑制因子,RORA激活抑制胶质瘤的细胞增殖和肿瘤发生。此外,昼夜节律紊乱与黑素瘤免疫逃逸有关。然而,节律基因在肿瘤免疫中的具体作用和机制少有报道,阐明节律基因调控抗肿瘤免疫的作用机制能为改善黑素瘤免疫治疗提供新思路。
在本项研究中,作者首先利用自测与公共数据库分析发现关键节律基因RORA与黑素瘤免疫相关,通过体内、外实验证实RORA在黑素瘤细胞、组织中显著低表达,并发挥细胞毒性T细胞活性依赖的抗肿瘤生长作用。机制研究表明,RORA通过与CD274启动子上特定位点结合,抑制了PD-L1的转录表达,并通过负调控PD-L1激活细胞毒性T细胞的抗肿瘤作用。此外,该节律分子通过招募HDAC3形成抑制复合体调控PD-L1的转录表达,相反,DEAD-box解旋酶家族成员DDX3X与HDAC3竞争结合RORA,其过表达促进RORA从抑制复合体及CD274启动子上释放,从而增加PD-L1的转录表达,产生免疫抑制作用。在治疗方面,本研究首次提出RORA激动剂川陈皮素(nobiletin)联合CTLA4抗体协同抑制肿瘤生长的治疗方案。总之,这项研究阐明了节律分子调节抗肿瘤免疫的新机制,表明RORA是改善黑素瘤患者免疫治疗反应的潜在靶点和预测性生物标志物。
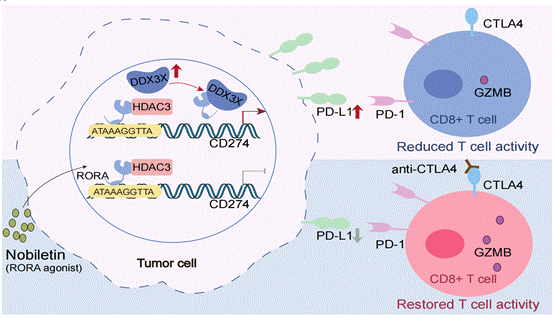
节律分子RORA通过抑制PD-L1表达增强黑素瘤免疫监视模式图
中南大学生命科学学院博士生刘丹丹、湘雅医院博士生魏本亮为本论文并列第一作者。中南大学生命科学学院刘静教授、刘雄昊教授以及湘雅医院陈翔教授、刘洪教授为本论文共同通讯作者。本研究受到科技部国家重点研发项目、国家自然科学基金重点课题等基金资助。
初稿:刘丹丹,一审:孙星,二审:胡艺俏,三审:陈超